Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1© és Concetta Lotti 2,*
- 1 Talaj-, Növény- és Élelmiszertudományi Tanszék, Növénygenetikai és Nemesítési Egység Bari Egyetem, Via Amendola 165/A, 70125 Bari, Olaszország; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (KAR); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Mezőgazdasági, Élelmiszer- és Környezettudományi Tanszék, Foggia Egyetem, Via Napoli 25, 71122 Foggia, Olaszország
- 3 Biotudományok, Biotechnológiák és Biogyógyszerészeti Tanszék, Bari Egyetem, Via Orabona 4, 70125 Bari, Olaszország; guglielmo.rainaldi@uniba.it
- 4 Energiatechnológiai Tanszék, Bioenergia, Biofinomító és Zöld Kémiai Osztály, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Olaszország; paolo.iovieno@enea.it
* Levelezés: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Absztrakt:
Hagyma (Allium cepa L.) a második legfontosabb zöldségnövény világszerte, és széles körben értékelik egészségügyi előnyei miatt. Jelentős gazdasági jelentősége és funkcionális élelmiszerként betöltött értéke ellenére a hagymát kevéssé vizsgálták genetikai sokfélesége tekintetében. Itt felmértük az „Acquaviva vöröshagyma” (ARO) genetikai variációját, egy évszázados termesztési múlttal rendelkező tájfajtát Bari tartomány (Apulia, Dél-Olaszország) kisvárosában. 11 mikroszatellit markert használtak a genetikai variációk feltárására egy 13 ARO populációból és három általános kereskedelmi típusból álló csíraplazma gyűjteményben. A genetikai szerkezet parametrikus és nem paraméteres módszerekkel végzett elemzése rávilágított arra, hogy az ARO egy jól meghatározott génállományt képvisel, amely egyértelműen különbözik a Tropea és Montoro tájfajtáktól, amelyekkel gyakran összetévesztik. Az általában friss fogyasztásra használt hagymák leírása érdekében kiértékeltük az oldható szilárdanyag-tartalmat és a csípősséget, ami az ARO-ban magasabb édességet mutatott a fent említett két tájfajtához képest. Összességében ez a tanulmány hasznos az ARO jövőbeli felértékelődése szempontjából, amelyet minőségi címkékkel lehetne előmozdítani, amelyek hozzájárulhatnak a kereskedelmi csalások korlátozásához és a kistermelők jövedelmének javításához.
Bevezetés
Az Allium nemzetség mintegy 750 fajt foglal magában [1], amelyek közül a vöröshagyma (Allium cepa L., 2n = 2x =16) az egyik legelterjedtebb. Az A. cepa kétévenkénti ciklusú, és átnyúló szaporodási viselkedést mutat. Napjainkban a hagyma globális termelése (97.9 Mt) a paradicsom után a második legfontosabb zöldségnövénysé teszi [2]. A hagymahagymákat ősidők óta élelmiszerként és népi gyógyászati célokra is használták. Valójában az ókori egyiptomiak már számos, a fokhagyma és a hagyma felhasználásán alapuló gyógyászati formuláról beszámoltak egy Kr.e. 1550-ből származó orvosi papiruszban, a Codex Ebers-ben [3].
Ezt a sokoldalú és egészséges zöldséget nyersen, frissen vagy feldolgozott termékként fogyasztják, és számos étel ízének fokozására használják. Számos közelmúltbeli tanulmány állítja, hogy a hagyma fogyasztása csökkentheti a szív- és érrendszeri betegségek [4,5], az elhízás [6], a cukorbetegség [7] és a rák különböző formáinak kockázatát [8–10]. A hagyma egészségügyi tulajdonságait gyakran a tápanyagok két osztályának magas szintjének tulajdonítják: a flavonoidoknak és az alk(en)il-cisztein-szulfoxidoknak (ACSO-knak). Az első osztályba tartoznak a flavonolok és az antocianinok. A kvercetin a fő kimutatható flavonol, amely erős antioxidáns és gyulladáscsökkentő tulajdonságairól ismert a szabad gyökök megkötésében és az átmeneti fémionok megkötésében. [11]; míg az antocianinok vörös/lila színt adnak egyes hagymafajtáknak. Ami az ACSO-kat illeti, a legnagyobb mennyiségben előforduló izoalliin [(+)-transz-S-1-propenil-L-cisztein-szulfoxid] [12], a sejtekben raktározott, nem illékony és nem fehérjetartalmú kén aminosav, amely közvetve felelős a hagyma csípős illatáért és ízéért [13]. A szövetek felbomlásakor az izoalliint az alliináz enzim hasítja, így egy sor illékony vegyület (piruvát, ammónia, tioszulfonátok és propánetiális S-oxid) keletkezik, amelyek szakadást és kellemetlen szagot (szúrós) okoznak. [14]. A hagyma csípősségét gyakran a hidrolízis során keletkező piroszőlősav mennyiségeként mérik a friss tömeg grammjában. [15, 16].
A Földközi-tenger medencéjének országaiban az egyik másodlagos diverzitási központnak javasolták A. cepa [17, 18], a hagymahagymák alakja, mérete, színe, szárazanyag-tartalma és csípőssége igen változatos [19-egy]. Ezenkívül a kénalapú műtrágyázás, agronómiai gyakorlatok, a talaj típusa, az éghajlati viszonyok és a fajták vagy tájfajták genotípusa sajátos érzékszervi és tápértékek biztosításával befolyásolhatja a hagyma minőségét. [23-egy]. Olaszországban a hagyma csíraplazmájának széles köre ellenére gyakran csak néhány hagymafajtát vizsgálnak tudományosan és jellemeznek megfelelően. [28, 29].
Az agrobiodiverzitás alapos genetikai és fenotípusos jellemzése kulcsfontosságú a növényi genetikai erőforrások megfelelő megőrzésének biztosításához és a specifikus genotípusok felhasználásának elősegítéséhez az értékláncban. [30-egy]. Az egyszerű szekvencia ismétlődő (SSR) markereket gyakran választották a térképezéshez [33-egy], DNS-ujjlenyomat és fajtadiszkrimináció [36-egy]és a genetikai variabilitás megbízható becslése a tájfajtákon belül és között [39-egy], mivel lokuszspecifikusak, több allélikusak, kodominánsan öröklődnek, nagymértékben reprodukálhatók és alkalmasak automatizált genotipizálásra.
Jelen tanulmányunkban figyelmünket egy pugliai hagyományos tájfajtára, az „Acquaviva vöröshagymára” (ARO) összpontosítottuk, amelyet ökológiai gazdálkodási módszerek szerint termesztenek a Bari tartományban található Acquaviva delle Fonti város egy kis területén. (Apulia, Dél-Olaszország). Ennek a tájfajtának a hagymái nagyok, laposak és vörös színűek, és nagyrészt helyi receptekben használják. Bár az ARO elnyerte a „Slow Food Presidium” minőségi védjegyet, előállítása tovább népszerűsíthető és védhető olyan európai uniós minőségi védjegyekkel, mint az oltalom alatt álló földrajzi jelzés (OFJ) és az oltalom alatt álló eredetmegjelölés (POD), mivel ezek hozzájárulhatnak a a kereskedelmi csalások és a kistermelők jövedelmének javítása. Itt az SSR molekuláris markereket hatékony eszközként használták az ARO-populációk közötti genetikai variációk felmérésére, és ennek a tájfajnak a megkülönböztetésére a másik két dél-olasz lilahagyma tájfajtától. Továbbá becsültük a csípősséget és az oldható szilárdanyag-tartalmat, hogy az ARO ízét a piaci kereslethez viszonyítva értékeljük.
Eredmények
Az Acquaviva vöröshagyma csíraplazma gyűjtemény létrehozása és morfológiai jellemzése
A BiodiverSO Apulia Region projekt keretében gazdálkodók által adományozott ARO tájfaj 13 populációjának magjait felhasználták az ARO csíraplazma gyűjtemény létrehozásához.
A hagymával, bőrrel és hússal kapcsolatos morfológiai leírókat ARO csíraplazmán és három vöröshagyma tájfajon gyűjtöttük, kettő a „Tropea vöröshagyma” (TRO), egy pedig a „Montoro copper onion” (MCO) tájfajtához (ábra) 1). Az összes ARO izzó lapos volt, és vörös külső héj és hús jellemezte őket a vörös különböző árnyalataival. Ezzel szemben a TRO izzók húsa teljesen piros volt, míg az MCO hagymák húsa gyengén pigmentált (S1 táblázat). A biokémiai elemzés lehetővé tette a szilárdanyag-tartalom és a csípősség értékelését. Amint azt a táblázat tartalmazza 1, A hagymák oldható szilárdanyag-tartalmának átlagértéke az ARO populációkban 7.60 volt, és 6.00 (ARO12) és 9.50° Brix (ARO11 és ARO13) között mozgott. Ez az érték magasabb volt, mint a TRO és MCO tájfajtákra becsült érték (4.25 és 6.00° Brix).

Táblázat 1. Az „Acquaviva Red Onion” (ARO), a „Trope Red Onion” (TRO) és a „Montoro Copper Onion” (MCO) populációkban értékelt szilárdanyag-tartalom és csípősség értékek *.
| KÓD | Oldható szilárdanyag tartalom (Brix) | Szúrósság (pmolg-1 FW) | ||
| Jelenteni | CV y (%) | Jelenteni | CV y (%) | |
| ARO1 | 6.25 D* | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 a | 22.98 |
| ARO3 | 7.50 XNUMX XNUMX BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.97 a | 3.74 |
| ARO 5 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.80 a | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 a | 3.49 |
| ARO9 | ABC 8.25 | 4.28 | 6.84 a | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | 9.50 A | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | 9.50 A | 7.44 | 6.63 a | 24.93 |
| Orlando | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
* Az azonos betűket kis- vagy nagybetűs átlagok statisztikailag nem különböznek egymástól 0.01P-nél, illetve 0.05P-nél (SNK teszt). y Variációs együttható.
Az ARO csípősségének átlagos értéke a piroszőlősav-tartalom alapján 6.00 volt, 4.51 pmol g között változott.-1 FW (ARO6) – 7.04 (ARO8). Ez az érték magasabb volt, mint a TRO és MCO tájfajtáknál becsült érték (3.54 pmol g-1 FW és 4.18 pmol g-1 FW, ill.
SSR polimorfizmus és genetikai kapcsolatok a csatlakozások között
Jelen tanulmányban a 11 vizsgált SSR primer kombinációból 37 egylókuszos polimorfizmust eredményezett, azaz legfeljebb két amplifikációs terméket eredményezett egyetlen egyedben. Összességében 55 allélt mutattak ki 320 egyénben, a lókuszonkénti allélok száma 2 (ACM147 és ACM 504) és 11 (ACM132) között volt, és átlagos értéke 5 allél volt (táblázat). 2). Az egyes populációkban az allélok száma (Na) 1.94 (ACM147 és ACM504) és 5.38 (ACM132) között, míg az allélek effektív száma (Ne) 1.41 (ACM152) és 2.82 (ACM449) között mozgott. Eltérések A Na és Ne értékek közötti különbség a populációkban alacsony gyakoriságú allélek jelenlétének és csak néhány allél túlsúlyának köszönhető. A legmagasabb megfigyelt heterozigóta (Ho) értéket az ACM138 és az ACM449 esetében emeltük ki (0.62), míg a legalacsonyabbat az ACM152-nél (0.25). A várható heterozigótaság (He), amely megfelel az elméleti elvárásnak panmiktikus populációban, 0.37 (ACM504) és 0.61 (ACM132, ACM138 és ACM449) között mozgott. A Wright-féle fixációs index (Fis) nullához közeli értékeket (átlag 0.05) jelenített meg az összes marker esetében, hasonló értékeket jelezve a megfigyelt és a várható heterozigóta szint között, mint az egy keresztező fajnál várható. Az egyes SSR markerek hatékonyságát a genetikai ujjlenyomatvételben a polimorf információtartalom-index (PIC) alapján becsülték meg, átlagosan 0.48-as értékkel, és 0.33 (ACM504) és 0.67 (ACM132) között változott. Egy másik hatékonysági index, a Shannon információs indexe (I) 0.84-es átlagértéket mutatott, és a feltételezett értékek 0.45 (ACM152) és 1.20 (ACM132) között mozogtak.
Táblázat 2. Az ARO, TRO és MCO populációk genetikai sokféleségének becslésére használt 11 SSR marker polimorfizmus jellemzői. Az allélok teljes száma (Na), a sávméret-tartomány és a polimorf információtartalom-index (PIC) Tekintse meg az ebben a vizsgálatban genotipizált, összesen 320 egyedből álló készletet. Allélek száma (Na), hatékony allélek száma (Ne), megfigyelt heterozigótaság (Ho), várható heterozigótaság (He), rögzítési index (F)is), és a Shannon információs indexe (I) 16 populációból számított átlagértékekre vonatkozik, amelyek mindegyikét 20 egyén alkotja.
| Locus. | Összes Na | Mérettartomány (bp) | PIC | Jelenteni | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Jelenteni | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
A populációk közül az ARO3, ARO6, ARO8, ARO10, TRO1 és MCO magas szintű genetikai variációt mutatott (Ho > 0.5), míg a legalacsonyabb diverzitást az ARO7 populációban figyelték meg (Ho = 0.27) (S2 kiegészítő táblázat). Összességében az összes csatlakozás F-et mutatottis nullához közeli értékek (Fis átlagérték = 0.054), amint az véletlenszerű párzási körülmények között várható.
A molekuláris variancia és a genetikai szerkezet elemzése
A genetikai variáció populációk közötti és azon belüli hierarchikus felosztását az AMOVA számította ki. Az eredmények rávilágítottak a populációkon belüli genetikai variációk jelentős hányadára (87%). A populációk közötti eltérés, 13%, rendkívül jelentős volt (P < 0.001) (Táblázat 3). A Wright-féle Fst fixációs indexhez hasonló, 0.002 (ARO2/ARO10) és 0.468 (ARO7/TRO2) közötti tartományban lévő Fpt paraméter páronkénti értékei szignifikánsak voltak (P < 0.05, 3), kivéve kilenc páronkénti összehasonlítást (SXNUMX kiegészítő táblázat).
Táblázat 3. 320 genotípus molekuláris variancia elemzése 16 populációból Allium cepa L.
| forrás | df | Négyzetek összege | Varianciabecslés | Szórás (%) | Fpt | P |
| A lakosság körében | 15 | 458.63 | 1.16 | 13% | ||
| Populációkon belül | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Végösszeg | 319 | 2731.62 | 8.66 |
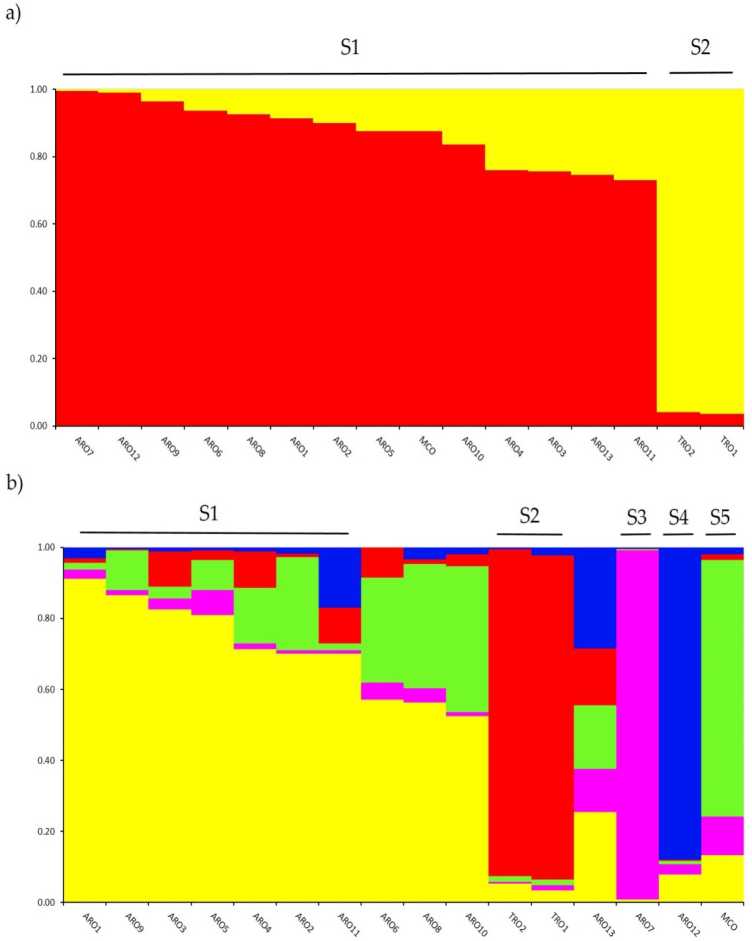
A genetikai szerkezet vizsgálata a A. cepa A jelen tanulmányban genotipizált kollekciót a STRUCTURE szoftverben megvalósított admixture modell alapú klaszterezési analízis segítségével végeztük. Az Evanno AK módszer a két klaszterre való felosztást javasolta (K = 2), mint a leginformatívabb számunkra. adatbázisba,th-vele következő legmagasabb peak K-nál = 5 (kiegészítő Rgure S1). A Villa = 2, ahpopulations were szamárigned isnésf a két klaszter val vel a rnernbertoip együttható (q) > 0.7. Mint shown be Ábra 2a, az első klaszter (S1 néven) az MCO és az összes ARO populációt tartalmazta, míg az S2 klaszter a két TRO populációt csoportosította. K = 5 esetén az adatkészlet mélyebb leírása (ábra 2b), a csatlakozások 75%-a az öt klaszter valamelyikébe került. Az ARO (S1) és a TRO (S2) szétválasztása megerősítést nyert, bár néhány ARO populációt összekevertek (q < 0.7) vagy külön csoportosítottak a két új S3 és S4 klaszterben (ARO7 és ARO12). Érdekes módon az MCO kereskedelmi típus különálló klasztert (S5) alkotott, amely elkülönült az apuliai vöröshagymától.
Genetikai kapcsolatok a populációk között
Az SSR polimorfizmus lehetővé tette a genetikai diverzitás dendrogramjának megrajzolását, és a filogenetikai elemzés eredményeit az ábra mutatja. 3a. Itt a csíraplazma gyűjteményt öt csoportra osztották, amelyet erősen támogattak a bootstrap értékek. Az ARO7 és ARO12 populációkat azonnal elválasztották a többi populációtól, és két különálló klasztert alkottak. A harmadik klaszter a TRO két kereskedelmi populációját foglalta magában, míg a negyedik csomópont tizenegy ARO populációból osztotta fel az MCO-t. A populációk között előforduló genetikai kapcsolatokat főkoordináta-analízissel (PCoA) tovább vizsgáltuk (ábra 3b). Amint azt korábban kiemeltük, az ARO-populációkat szorosan csoportosították, kivéve az ARO12-t és az ARO7-et, amelyek elszigetelt pozíciókban jelentek meg a PCoA diagramon. A két TRO és az MCO populáció a telek jobb alsó paneljén volt szétszórva.
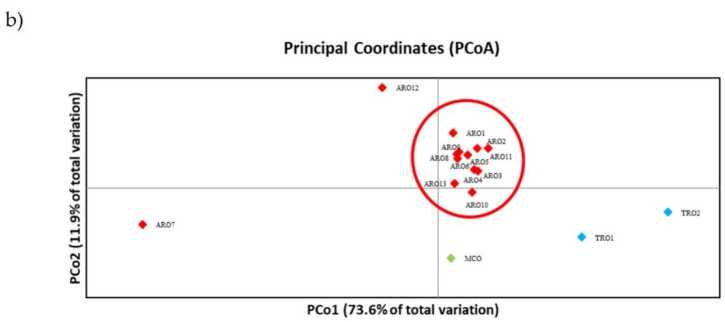
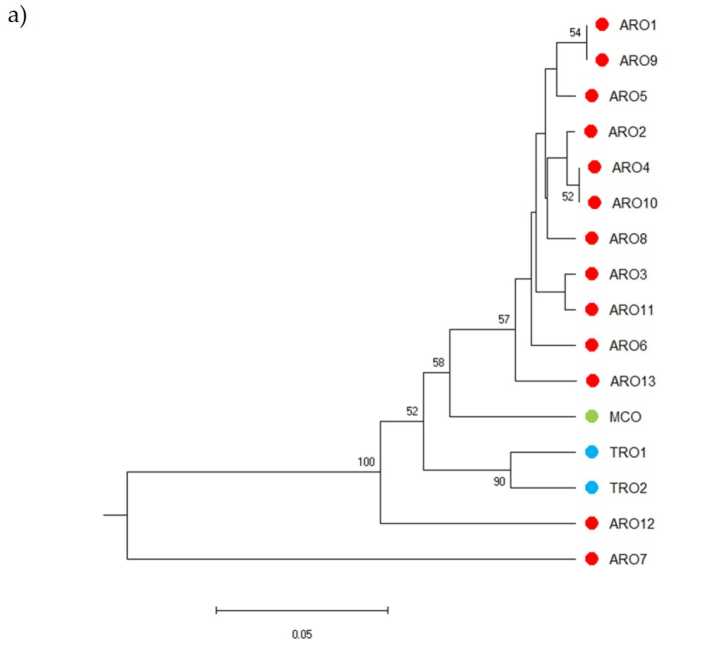
Ábra 3. Genetikai sokféleség a 16 között A. cepa a tanulmányban jellemzett populációk SSR-profilja alapján. (a) A genetikai távolság UPGMA dendrogramja. Az 50-nél nagyobb Bootstrap támogatási értékek a megfelelő csomópontok felett vannak feltüntetve; (b) főkomponens-elemzés (PCoA). A pirossal bekarikázott klaszter teljes mértékben megfelelt a filogenetikai analízis által generált és 11 ARO-csatlakozásból álló csoportnak.
Megbeszélés
A Dél-Olaszországban hagyományosan termesztett nagy mennyiségű mezőgazdasági biodiverzitáson belül a hagymás tájfajták olyan réstermékeket képviselnek, amelyeket meg kell őrizni a genetikai erózió kockázatától és a modern fajtákkal való helyettesítés veszélyétől. A BiodiverSO regionális projekt keretében, melynek célja az Apulia régióban a helyi örökséghez erősen kötődő genetikai erőforrások összegyűjtése, jellemzése, népszerűsítése és megőrzése, 13 ARO tájfajtából álló maggyűjteményt hoztunk létre. Beszámoltunk az ARO variáció első értékeléséről a DNS-polimorfizmusok és két biokémiai paraméter, az oldható szilárdanyag- és piroszőlősav-tartalom tekintetében, amelyek az ízjegyekkel kapcsolatosak és fontosak a friss, nyers termékek elfogadása szempontjából. Ezenkívül az ARO tájfajtára vonatkozó adatokat összehasonlították két másik, pigmentált hagymás tájfajtán gyűjtött adatokkal, amelyekkel gyakran tévedett.
A biokémiai elemzések rávilágítottak a 13 ARO-populáció édességére, amely a magas oldhatóanyag-tartalomhoz és a közepes csípősséghez kapcsolódik, az édeshagyma-ipari irányelvek szerint. [31]. Az ARO izzók édesebbek voltak, mint a TRO és MCO tájfajtáké, és valamivel nagyobb csípősséget mutattak. A vöröshagyma édessége azonban a cukortartalom és a csípősség egyensúlyának köszönhető, ezért ez a jellemzés hasznos lehet az értékes genotípusok kiválasztásához, amelyet általában csak a morfológia alapján végeznek a gazdák.
Bebizonyosodott, hogy az SSR markerek hasznos eszközei a genotípusok megkülönböztetésének, jóllehet szűk termőterületen, például Acquaviva delle Fonti városában gyűjtötték őket. A kiválasztott markerek több allélt mutattak, mint a korábban bejelentett markerek [43] és a [44], de alacsonyabb, mint az általa jelentett jelzők [45]. Ezen túlmenően a markereink 50%-a 0.5-nél nagyobb PIC-index értéket mutatott, ami alkalmasnak bizonyult a gyűjteményben lévő populációk megkülönböztetésére, amint azt a szerző javasolja. [46]. A populációkon belüli diverzitás értékelése hasonló értékeket mutatott ki Ho és He között, ami alacsony Fi-értéket eredményezetts értékeket. Ez összhangban van a kilépési jellegével A. cepa, amely súlyosan szenved a beltenyésztés depressziójában [47]. Az általános Fis a vizsgálatban figyelembe vett hagymapopulációkban számított érték (0.054) alacsonyabb volt, mint a korábban közölt érték. [45] (0.22) és majdnem megegyezik a által találttal [31] (0.08) és [48] (0.00), akik az északnyugat-spanyolországi és nigeri hagyma tájfajták genetikai sokféleségét értékelték. Az ARO-populációk figyelemre méltó heterozigóta szintje megerősíti azt az elképzelést, hogy Apulia sok kertészeti faj diverzitási központja. [32, 42, 49-egy].
Az AMOVA kiemelte, hogy az ebben a tanulmányban genotipizált gyűjteményben a legtöbb molekuláris variáció a populációkban rejlik. A populációk közötti jelentős genetikai differenciálódás azonban (FPT értékek) feltárták a genetikai rétegződés előfordulását. Valójában, bár eredményeink azt mutatták, hogy a legtöbb ARO populációban a genetikai egységesség jelen van, jól meghatározott klasztert alkotva, az ARO7 és ARO12 populációk egyértelműen eltérő genetikai profilt mutattak. Ez az eredmény a két gazda által használt vetőmagok eltérő eredetének tudható be, akiktől a populációkat gyűjtötték. Sőt, a kapott eredmények alapján az ARO tájfajtát genetikai szinten egyértelműen megkülönböztethetjük a TRO és MCO tájfajtáktól. Egy friss tanulmányban [29] felmérte több olasz hagymás tájfajtát, köztük az „Acquaviva”, a „Tropea” és a „Montoro” genetikai sokféleségét. Bár a szerzők SNP-markereket használtak egy szélesebb hagymagyűjtemény genetikai diverzitásának felmérésére, a genotipizálás nem tudta megkülönböztetni az „Acquavivát” a „Tropea” és a „Montoro” hagymától. Valószínűleg ez az eltérés az alacsony átlagos PIC értéknek köszönhető (0.292), ami az elemzett lókuszok szerény általános informativitására utal, ahogy azt állítja. [29]. Ezen túlmenően, annak érdekében, hogy megvizsgálhassuk az alstruktúrák jelenlétét olasz klaszterükben, jobb lett volna az olasz genotípusokat a gyűjtemény többi részétől elkülönítve elemezni. Valószínűleg lehetővé tette volna a genetikai sokféleség mintázatának megjelenítését, amely a földrajzi rétegződéshez vagy az empirikus szelekció során jellemző tulajdonságokhoz kapcsolódik.
Összefoglalva, ez a tanulmány egy átfogó jelentés a helyi kulturális örökséghez kapcsolódó és a gazdálkodók számára gazdasági jelentőségű hagymás tájfajtáról. Eredményeink rávilágítanak arra, hogy néhány kivételtől eltekintve az ARO-t jól körülhatárolható génállomány jellemzi, amelyet érdemes megóvni a genetikai erózió kockázatától. Ezért kulcsfontosságú volt a genetikai sokféleség ezen értékes forrásának reprezentatív gyűjteményének létrehozása. Végül az ARO genetikai és fenotípusos jellemzése hasznos lehet az Európai Unió minőségi védjegyeinek megszerzéséhez.
Anyagok és módszerek
Csíraplazma gyűjtés, növényi anyagok és DNS kivonás
Az ARO tájfajták 13 populációját egy Puglia régió projekt (BiodiverSO:) keretében szereztük be. https://www.biodiversitapuglia.it/), az olaszországi Bari tartomány kisvárosában, az „Acquaviva delle Fontiban” végrehajtott küldetések sorozatán keresztül. Az egyes csatlakozások gyűjtőhelyeit a Földrajzi Információs Rendszeren (GIS) térképezték fel, és a táblázatban jelentették 4. Ezen túlmenően, két populációt a TRO tájfajtából és egy populációt az MCO tájfajból vettünk be a jelen tanulmányba, és referenciaként használtuk. Az összes növényi anyagot azonos környezeti körülmények között termesztették a Bari Egyetem „P Martucci” kísérleti farmján (41° 1'22.08″ é. 16°54'25.95″ K), védőketrecben a keresztbeporzás elkerülése érdekében. populáción belüli beporzást a légy segítségével (Lucilia caesar). A 16 populációt a hagyma méretével és alakjával, valamint a bőr és a hús színével kapcsolatos tulajdonságok alapján jellemeztük (S1 táblázat). Ezenkívül kézi refraktométerrel szilárdanyag-oldható tartalom meghatározást végeztünk, és hagymalé minták csípősségét 2,4-dinitrofenil-hidrazin (0.125%) hozzáadásával mértük. v/v 2 N HCl-ben) és 420 nm-en mérjük az abszorbanciát, amint azt a [31]. A szignifikáns különbségek meghatározására a Duncan-féle több tartományú tesztet és az SNK-tesztet végeztük.
Táblázat 4. A tanulmányban összegyűjtött és genotipizált populációk listája. Minden populáció esetében jelenteni kell az azonosító kódot, a helyi nevet, a GPS-koordinátát és a magokat megőrző génbankot.
| Kód | Név | GPS koordináták | Génbank y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54"51.372″ N 16°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52"49.8″ N 16°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| Orlando | Cipolla rama di Montoro | - | Di.SSPA |
| y Di.SSPA, Talaj-, Növény- és Élelmiszertudományi Tanszék, Bari Egyetem. |
Populációnként 20 genotípus levélanyagából mintát vettünk, és felhasználásig -80 °C-on tároltuk. A poliszacharidokban gazdag fajokhoz, mint A. cepa, A poliszacharid eltávolításának első lépései nélkülözhetetlenek a jó minőségű DNS előállításához, ezért a kezdeti mosásokat STE pufferben (0.25 M szacharóz, 0.03 M Tris, 0.05 M EDTA) a következő leírás szerint végeztük: [52]. A teljes DNS-t CTAB módszerrel extraháltuk [53] végül Nano Drop 2000 UV-vis spektrofotométerrel (ThermoScientific, Waltham, MA, USA) és 0.8%-os agaróz gélelektroforézissel ellenőriztük a minőséget és a koncentrációt.
SSR elemzés
16 EST-SSR primer kombinációt fejlesztett ki [54] és korábban a genetikai diverzitás vizsgálataiban tesztelték [43] és a [44] és 21 genomiális SSR [45-egy] szűrték, hogy értékeljék alkalmasságukat (S4 kiegészítő táblázat). A genotipizálást a gazdaságos fluoreszcens címkézési módszerrel végeztük, amelyben az M13 farok minden egyes előremenő SSR primerhez hozzáadódik. [56]. A PCR keverékeket 20 gl-es reakcióban állítottuk elő, amely a következőket tartalmazta: 50 ng teljes DNS, 0.2 mM dNTP keverék, 1X PCR reakciópuffer, 0.8 U DreamTaq DNS polimeráz (Thermo Scientific, Waltham, MA, USA), 0.16 g reverz primer. 0.032 gM M13 szekvenciával kiterjesztett előremenő primer (5'-TGTAAAACGACGGCCAGT-3') és 0.08 gM univerzális M13 primer, amelyet FAM vagy NED fluoreszcens festékekkel jelöltek (Sigma-Aldrich, St. Louis, MO, USA). A PCR-reakciókat SimpliAmp (Applied Biosystems, CA, USA) termociklerben végeztük a következő feltételekkel a legtöbb primerpár esetében: 94 °C 5 percig, 40 ciklus 94 °C-on 30 másodpercig, 58 °C 45 másodpercig és 72 °C-on 45 másodpercig, és végső megnyúlás 72 °C-on 5 percig. Ami az ACM446-ot és az ACM449-et illeti, touchdown PCR-t alkalmaztunk 60 °C és 55 °C közötti hőkezeléssel 10 cikluson keresztül, 30 cikluson keresztül 55 °C-on, majd 5 perces utolsó meghosszabbítást 72 °C-on. A PCR-termékeket 96 lyukú lemezre töltöttük, és 14 g Hi-Di Formamide-dal (Life Technologies, Carlsbad, CA, USA) és 0.5 g GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA) kevertük. Az amplikonokat ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA) kapilláris szekvenáló gép segítségével határoztuk meg, ahol az allélokat kodominánsnak értékeltük, és a GeneMapper Software 3.7-es verziójával rendeltük hozzá.
A szoftver GenAlEx 6.5 [57] és Cervus 3.0.7 [58] Az allélok számának (Na), a hatékony allélek számának (Ne), a megfigyelt heterozigótaságnak (Ho), a várható heterozigótaságnak (He), a polimorf információtartalomnak (PIC), a Shannon-féle információs indexnek (I) és a fixációs indexnek (Fis) becsülték meg. ) minden SSR-lókuszhoz.
A genetikai sokféleség felmérése
A genetikai variációk hierarchikus felosztását a hagymapopulációk között és azokon belül a GenAlEx 6.5 értékelte [57] a molekuláris variancia (AMOVA) elemzésén keresztül 999 bootstrapping segítségével a szignifikancia tesztelésére. Ezenkívül a GenAlEx 6.5 szoftvert használták az egyes populációk sokféleségének becslésére, a Ho, He és Fis átlagának kiszámításával az összes SSR-lókuszra vonatkozóan.
A populáció szerkezetére a STRUCTURE v.2.3.4 szoftverben megvalósított Bayes-féle modell alapú klaszterező algoritmus következtetett. [59]. Az adatkészletet számos hipotetikus klaszterrel (K) futtattuk, 1-től 10-ig, minden K-értékenként tíz független futtatást beállítva. Az eredmények konzisztenciájának ellenőrzése céljából minden egyes futtatásnál 100,000 100,000 kezdeti beégési időszakot és XNUMX XNUMX Markov Chain Monte Carlo (MCMC) iterációt hajtottak végre a keverékmodell és a populációk közötti független allélgyakoriságok alapján. A legvalószínűbb K értéket az általa leírt AK módszerrel határoztuk meg [60], a STRUCTURE HARVESTER web alapú programban [61]. Egy adott populációt akkor rendeltünk egy adott klaszterhez, ha a tagsági együtthatója (q-értéke) magasabb volt, mint 0.7, ellenkező esetben vegyes származásúnak tekintettük.
A fő koordináta-analízist a Nei genetikai távolságmátrixa által feltárt genetikai kapcsolatok mintáinak megjelenítésére végezték el a csatlakozások között (S5 kiegészítő táblázat). Az allélgyakoriságok alapján a POPTREEW szoftverben a súlyozatlan páros csoport módszert aritmetikai átlagokkal (UPGMA) klaszteranalízissel valósítottuk meg a genetikai távolság dendrogramját. [62]. A rendszerindítást alkalmaztuk a hierarchikus klaszterezés megbízhatóságának felmérésére, beállítva az adatkészlet 100-as újramintavételezését. Végül a MEGA X szoftver [63] farajzoló szoftverként használták.
Kiegészítő anyagok: A következők online elérhetők a következő címen: http://www.mdpi.com/2223-7747/9/2/260/s1. S1 táblázat: Az ARO, MCO és TRO izzók morfológiai jellemzése. S2 táblázat: ARO tájfajtákra, valamint TRO és MCO tájfajtákra számított heterozigótasági és fixációs indexek. S3 táblázat: Az Fpt paraméter páronkénti értékei. S4 táblázat: A tanulmányban használt SSR-ek listája. S5 táblázat. Nei genetikai távolság páronkénti populációmátrixa. S1 ábra: Evanno Delta K-vel változó K értékek vonaldiagramja.
Szerzői hozzájárulások: CL és LR tervezte a tanulmányt és tervezte meg a kísérletet; A CL és a PI molekuláris markeranalízist végzett; Az ARM és a VZ elvégezte a tereppróbákat; RM, SP, GR és CL vett részt az adatelemzésben; RM és CL írta a kéziratot. Minden szerző elolvasta és elfogadta a kézirat közzétett változatát.
finanszírozás: Ezt a munkát az „Apuliai zöldségfajok biodiverzitása” nevű regionális apuliai projekt – Programa di Sviluppo Rurale per la Puglia 2014–2020 – finanszírozta. Misura 10—Sottomisura 10.2; támogatás CUP H92C15000270002, Olaszország.
Köszönetnyilvánítás: Köszönet illeti az „Azienda Agricola Iannone Annát” és az „Associazione produttori della vera cipolla rossa di Acquaviva”-t a kísérletben felhasznált növényi anyagok biztosításáért.
Összeférhetetlenség: A szerzők nem jeleznek összeférhetetlenséget.
Referenciák
- 1. Stearn, WT Hány Alliumfaj ismert? Kew Mag. 1992, 9,180-182. [CrossRef]
- 2. FAOSTAT. FAO statisztikai adatbázis. Online elérhető: http://www.fao.org/2017 (Hozzáférés: 8. január 2019.).
- 3. Block, E. A fokhagyma és a hagyma kémiája. Sci. Am. 1985, 252,114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS A vöröshagyma antioxidáns aktivitásának értékelése patkányban. Food Chem. Toxicol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Moon, J.; Chung, JH; Cha, YJ; Shin, MJ A kvercetinben gazdag hagymahéj kivonatok hatása patkányok artériás trombózisára. Food Chem. Toxicol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. A hagymakivonat elhízás elleni hatásai cukorbeteg zsíros patkányokban. Tápanyagok 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehman, K.; Chen, S. Fűszernövény Allium cepa: Étrend-kiegészítő 2-es típusú diabetes mellitus kezelésére. Táplálás 2014, 30,1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF A hagyma gátló hatásai (Allium cepa L.) kivonat a rákos sejtek és zsírsejtek proliferációjára a zsírsavszintáz gátlásával. Ázsiai Pac. J. Cancer Prev. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Lien, JC; Tsai, CH; Chung, JG Quercetin gátolja a SAS humán szájrákos sejtek migrációját és invázióját az NF-kappaB és a mátrix metalloproteináz-2/-9 jelátviteli útvonalak gátlásán keresztül. Anticancer Res. 2013, 33,1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Fokhagyma és hagyma: rákmegelőző tulajdonságaik. Rák Előz. Res. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. A kvercetinnel funkcionalizált hidroxiapatit antioxidáns és csontjavító tulajdonságai: In vitro oszteoblaszt-oszteoklaszt-endoteliális sejt-kokultúra vizsgálat. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Tizenegy íz-prekurzor, S-Alk(en)il-L-cisztein származékok eloszlása hét Allium zöldségben. Food Sci. Technol. Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Az Allium nemzetség szerves kénkémiája – A kén szerves kémiájára gyakorolt hatás. Angew. Chem. Int. Szerk. Engl. 1992, 31,1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Thomas, B.; Smith, B. Hagyma – Globális egészségügyi előny. Fitother. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Piroszőlősav enzimatikus fejlődése hagymában a csípősség mértékeként. J. Agric. Élelmiszer chem. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CAT; Randle, WM Szúrósság értékelése hagymában. Ban ben Tesztelt tanulmányok laboratóriumi oktatáshoz; Karcher, SJ, szerk.; Association for Biology Laboratory Education (ABLE): New York, NY, USA, 1998; 19. évfolyam, 177-196.
- 17. Hanelt, P Taxonómia, evolúció és történelem. Ban ben Onions and Allied Crops, Vol. I. Botanika, élettan és genetika; Rabinowitch, HD, Brewster, JL, szerk.; CRC Press: Boca Raton, FL, USA, 1990; 1-26.
- 18. Rabinowitch, HD; Currah, L. Allium Crop Science: Recent Advances; CABI Kiadó: Wallingford, Egyesült Királyság, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. A hagyma genetikai erőforrásainak jellemzése (Allium cepa L.) a spanyol másodlagos diverzitásközpontból. Span. J. Agric. Res. 2011, 9,144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Fenolok és cisztein-szulfoxidok értékelése helyi hagyma és mogyoróhagyma csíraplazmában Olaszországból és Ukrajnából. Közönséges petymeg. Erőforrás. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. A „vatikiotiko”, egy görögországi hagymás helyi faj morfológiai, táplálkozási és kémiai leírása. Food Chem. 2015,182,156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Különböző hagymafajták biokémiai, antioxidáns tulajdonságai és antimikrobiális hatása a mediterrán térségben. J. Food Meas. Karakter. 2019,13,1232-1241. [CrossRef]
- 23. Yoo, KS; Pike, L.; Crosby, K.; Jones, R.; Leskovar, D. Különbségek a hagyma csípősségében a fajták, a növekedési környezet és a hagymaméretek miatt. Sci. Hortic. 2006,110,144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; George, E.; Kroh, LW; Rohn, S. A kvercetin-3, 4'-O-diglükozid, kvercetin-4'-O-monoglükozid és kvercetin megoszlása a hagymahagyma (Allium cepa L.) különböző részein a genotípus hatására. Food Chem. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Az átültetési idő és a növénysűrűség hatása a hagyma hozamára, minőségére és antioxidáns tartalmára (Allium cepa L.) Dél-Olaszországban. Sci. Hortic. 2014,166,111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF A hagyma hozzáadott értékének növelése az antioxidáns flavonoidok forrásaként: kritikai áttekintés. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. A termesztési módszer és a fajtaválasztás hatása az oldható szénhidrátokra és a csípős elvekre hagymában (Allium cepa L.). J. Agric. Élelmiszer chem. 2018, 66,12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Két dél-olaszországi fajtából származó flavonoidok azonosítása és mennyiségi meghatározása Allium cepa L., Tropea (vörös hagyma) és Montoro (rézhagyma), valamint az emberi vörösvértestek oxidatív stressztől való védelmére való képességük. J. Agric. Élelmiszer chem. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. A nagy áteresztőképességű genotipizálás a hagymában feltárja a genetikai sokféleség szerkezetét és a molekuláris nemesítésben használható informatív SNP-ket. Mol. Fajta. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Egy olasz hosszú eltarthatóságú paradicsom genetikai változata (Solanum lycopersicum L.) gyűjtése SSR és morfológiai gyümölcsjegyek felhasználásával. Közönséges petymeg. Erőforrás. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. A genetikai sokféleség és a minőségi jellemzők feltárása egy hagymagyűjteményben (Allium cepa L.) északnyugat-spanyolországi tájfajták. Genetika 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. A kelkáposzta genetikai, bio-agronómiai és táplálkozási jellemzése (Brassica oleracea L. var. acephala) sokszínűség Pugliában, Dél-Olaszországban. Sokféleség 2018,10, 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. A rezisztencia genetikai elemzése Orobanche crenata (Forsk.) borsóban (Pisum sativum L.) alacsony strigolakton vonal. J. Plant Pathol. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Kvantitatív jellemző lókuszok feltérképezése csavarozási időre fürtös hagymában (Allium fistulosum L.). Euphytica 2016, 209, 537-546. [CrossRef]
- 35. Daka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Genikus SSR-ek azonosítása és SSR-alapú kapcsolódási térkép felépítése in Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. A hagyma fajtaazonosságának értékelése SSR markerek segítségével. Seed Sci. Technol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. A Cseh Köztársaságból származó hagymafajták megkülönböztetésére szolgáló markerkészlet kiválasztása és validálása. cseh J. Genet. Növényfajta. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Az apuliai olajbogyó-csíraplazma biodiverzitásának megőrzése és jellemzése. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. A spanyol nyelv genetikai sokféleségének felmérése Allium cepa tájfajták hagymanemesítéshez mikroszatellit markerek segítségével. Sci. Hortic. 2014,170,24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. A hagymák genetikai sokféleségének felmérése (Allium cepa L.) északnyugat-spanyolországi tájfajták és összehasonlítás az európai változékonysággal. NZJ Crop Hortic. 2016, 44,103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan, S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. A csicseriborsó globális csíraplazmagyűjteményének genetikai variációja (Cicer arietinum L.) beleértve a genetikai erózió veszélyének kitett olasz csatlakozásokat is. Physiol. Mol. Biol. Növények 2017, 23,197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Genetic diversity in broccoli rabe (Brassica rapa L. subsp. sylvestris (L.) Janch.) Dél-Olaszországból. Sci. Hortic. 2019, 253,140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Egy nukleotid polimorfizmusok, indelek és egyszerű szekvenciaismétlések a hagymafajta azonosításához. J. Am. Soc. Hortic. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Genetikai diverzitáselemzés és egynukleotidos polimorfizmus markerek kifejlesztése termesztett hagymahagymában expresszált szekvencia-tag-egyszerű szekvenciaismétlési markerek alapján. J. Am. Soc. Hortic. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Robusztus genomiális egyszerű szekvencia-ismétlési markerek fejlesztése a hagymán belüli és a hagyma közötti genetikai diverzitás becslésére (Allium cepa L.) populációk. Mol. Fajta. 2012, 30,1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Microsatellite markerek fehérfarkú szarvasban. J. Hered. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. Iráni hagyma (Allium cepa L.) fajták beltenyésztési depresszióra adott válaszai. World Appl. Sci. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Niger hagyma genetikai sokfélesége (Allium cepa L.) egyszerű szekvencia ismétlési markerekkel (SSR) értékelték. Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; et al. Különleges genetikai klaszter a termesztett csicseriborsóban, amint azt az egész genomra kiterjedő markerek felfedezése és genotipizálása mutatta ki. Növényi genom 2017, 2017,10. [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. A dinnye genotipizálása szekvencia alapján (Cucumis melo L.) a diverzitás másodlagos központjából származó csíraplazma gyűjtemény rávilágít a genetikai variációs mintázatokra és a különböző génállományok genomikai jellemzőire. BMC Genom. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Genetikai áramlás az olajbogyó populáció között a Földközi-tenger medencéjében. Peer J. 2018, 6. [CrossRef]
- 52. Pásztor, LD; McLay, TG Két mikroléptékű protokoll DNS izolálására poliszacharidban gazdag növényi szövetből. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Növényi DNS izolálása friss szövetből. Összpontosít 1990,12,13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Mosogató, KC; Jenderek, M.; et al. A 11,008 XNUMX hagymás expresszált szekvencia-címkéből álló egyedülálló készlet felfedi az expresszált szekvencia és genomiális különbségeket az egyszikű spárgák és a poales rendek között. Növényi sejt 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Dal, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Marker fejlesztés a hagyma genetikai tisztaságának vizsgálatához az SSR Finder segítségével. Koreai J. fajta. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Egy gazdaságos módszer PCR-fragmensek fluoreszcens jelölésére. Nat. Biotechnol. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Genetikai elemzés Excelben. Populációgenetikai szoftver oktatáshoz és kutatáshoz: Frissítés. bioinformatikai 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Kúpos, ML; Marshall, TC A CERVUS számítógépes program genotipizálási hibáinak kezelési módjának felülvizsgálata növeli az apasági kijelölés sikerét. Mol. Ecol. 2007,16,1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Asszociációs térképezés strukturált populációkban. Am. J. Hum. Közönséges petymeg. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Egyedcsoportok számának kimutatása a szoftver segítségével STRUCTURE: A Simulation study. Mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. STRUCTURE HARVESTER: Weboldal és program a STRUCTURE output megjelenítésére és az Evanno módszer megvalósítására. Conserv. Közönséges petymeg. Erőforrás. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: A POPTREE webes változata populációs fák létrehozására allélgyakorisági adatokból és más mennyiségek kiszámításához. Mol. Biol. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Molekuláris evolúciós genetikai elemzés számítástechnikai platformokon. Mol. Biol. Evol. 2018, 35,1547-1549. [CrossRef]